第一章课后习题详解
1、(1)在0℃及101.325 kPa下,纯干空气的密度为1.293×10-3g·m-3,试求空气的表观摩尔质量;
(2)在室温下,某氮气钢瓶内的压力为538 kPa,若放出压力为100 kPa的氮气160 dm3,钢瓶内的压力降为132 kPa,试估计钢瓶的体积。设气体近似作为理想气体处理。
解:(1)根据理想气体状态方程,有
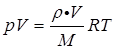
即
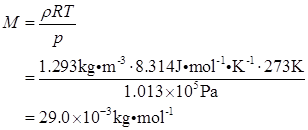
(2)根据Dalton分压定律,在相同体积,相同压力条件下,可得
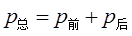

根据理想气体状态方程,在相同温度条件下,可得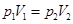 ,则
,则
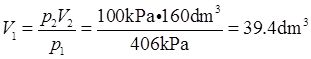
因此钢瓶体积为39.4dm3。
2、两个体积相同的烧瓶中间用玻管相通,通入0.7 mol氮气后,使整个系统密封。开始时,两瓶的温度相同,都是300 K,压力为50 kPa,今若将一个烧瓶浸入400 K的油浴内,另一烧瓶的温度保持不变,试计算两瓶中各有氮气的物质的量和温度为400 K的烧瓶中气体的压力。
解:两体积相同的烧瓶中,在温度为300K,压力为50kPa的条件下通入0.7mol氮气,则两烧瓶中均有0.7/2=0.35(mol)的氮气。
根据理想气体状态方程,烧瓶的体积为
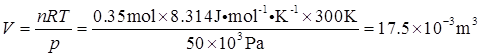
将一个烧瓶浸入400K油浴中,另一烧瓶保持300K。当两烧瓶平衡后,两烧瓶的压力相等,对应的两烧瓶体积也相等,设400K的烧瓶中氮气的物质的量为n1,300K烧瓶中氮气的物质的量为n2,则有
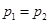

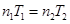
又因为充入氮气的总量为0.7mol,则n2=0.7-n1,代入上式得
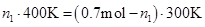
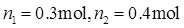
400K烧瓶中的压力为
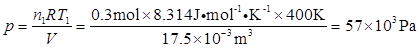
即400K烧瓶中氮气的物质的量为0.3mol,压力为57kPa,另一烧瓶中氮气的物质的量为0.4mol。
3、在293 K和100 kPa时,将He(g)充入体积为1 dm3的气球内。当气球放飞后,上升至某一高度,这时的压力为28 kPa,温度为230 K,试求这时气球的体积是原体积的多少倍?
解:在气球可承受范围内,将He(g)充入,此时气球内压力、温度均与外界相等,即p1=100kPa,T1=293K,V1=1dm3;当上升至某一高度,p2=28kPa,T2=230K时,根据理想气体状态方程,有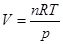 ,因此
,因此
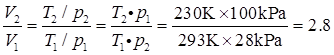
4、有2.0 dm3潮湿空气,压力为101.325 kPa,其中水气的分压为12.33 kPa。设空气中O2(g)和N2(g)的体积分数分别为0.21和0.79,试求
(1)H2O(g),O2(g),N2(g)的分体积;
(2)O2(g),N2(g)在潮湿空气中的分压力。
解:(1)在潮湿空气中,水气的分压为12.33kPa。
根据Dalton分压定律,有
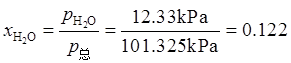
根据Amagat分体积定律,有
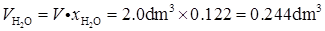
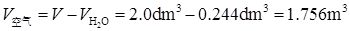
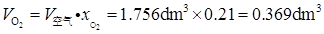
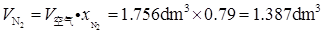
(2)由Dalton分压定律,知
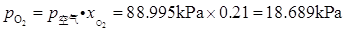
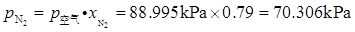

| 内容来源 |
傅献彩《物理化学》第5版课后习题答案 |
扫码阅读 |
5、3.459 H2(g)放在10 dm3的密闭容器中,从273 K加热到373 K,问需提供多少能量?H2(g)的根均方速率是原来的多少倍?已知H2(g)的摩尔等容热容Cv,m=2.5R。
解:已知H2(g)的摩尔等容热容Cv,m=2.5R,因H2在密闭容器中加热,所以能量为

由根均方速率公式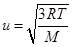 得
得
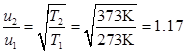
6、计算293 K和373 K时,H2(g)的平均速率、根均方速率和最概然速率。
解:在293K时,H2(g)的平均速率为

根均方速率为
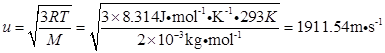
最概然速率为
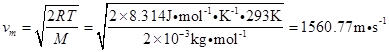
因此,有 。
。
同理,在373K时,有
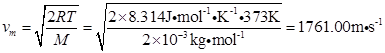
由 可得
可得

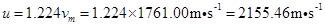
7、计算分子动能大于10 kJ的分子在总分子中所占的比例。
解:若在298K时有
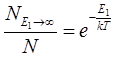
即
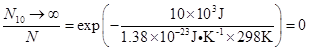
则分子动能大于10kJ的分子在总分子中几乎没有。
8、在一个容器中,假设开始时每一个分子的能量都是2.0×10-21J,由于相互碰撞,最后其能量分布适合于Maxwell分布。试计算:
(1)气体的温度;
(2)能量介于1.98×10-21J到2.02×10-21J之间的分子在总分子中所占的分数。(由于这个区间的间距很小,故用Maxwell公式的微分式)
解:(1)由题意可知,每一个分子的能量为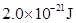 。
。
则1mol分子的平均平动能为
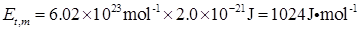
又因为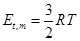 ,所以
,所以
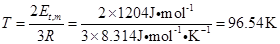
(2)由于各分子的能量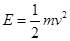 ,微分得dE=mvdv,代入下式
,微分得dE=mvdv,代入下式

可得
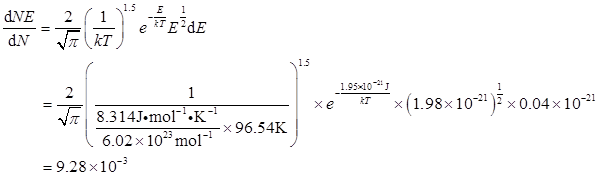
9、根据速率分布公式,计算分子速率在最概然速率以及大于最概然速率1.1倍(即dvm=0.1vm)的分子在总分子中所占的分数(由于这个区间的间距很小,可用微分式)。
解:分子速率在最概然速率 以及
以及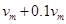 之间的分子在总分子中的所占分数为:
之间的分子在总分子中的所占分数为:
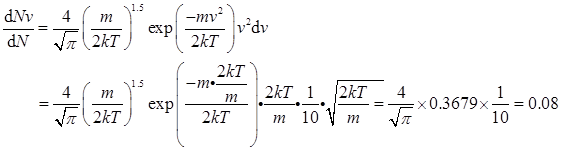
10、在293 K和100 kPa时,N2(g)分子的有效直径约为0.3 nm,试求
(1)N2(g)分子的平均自由程;
(2)每一个分子与其他分子的碰撞频率;
(3)在1.0 m3的体积内,分子的互碰频率。
解:(1)N2(g)分子的平均自由程只有一个分子移动,则其平均自由程为
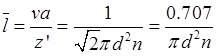
根据理想气体状态方程,有
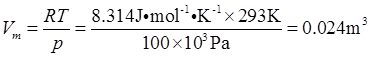
n为单位体积内的分子个数,所以
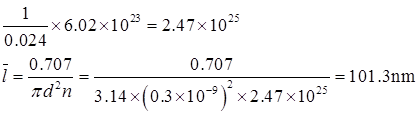
(2)由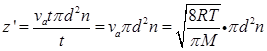 ,得每一个分子与其他分子的碰撞频率为
,得每一个分子与其他分子的碰撞频率为

(3)根据分子的互撞次数公式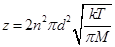 ,可得
,可得
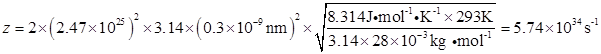
……
……
完整版链接: /Ebook/988472.html
【推荐】达聪学习网 “傅献彩《物理化学》(第5版)笔记和课后习题(含考研真题)详解”
热门文章
——————————————————————————————